 Phân bố electron trong nguyên tử bạc
Phân bố electron trong nguyên tử bạc
Cấu hình electron, hay cấu hình điện tử, nguyên tử cho biết sự phân bố các electron trong lớp vỏ nguyên tử ở các trạng thái năng lượng khác nhau hay ở các vùng hiện diện của chúng.
Số lượng tử và lớp[sửa|sửa mã nguồn]
Trạng thái của mỗi electron trong lớp vỏ hoàn toàn có thể được màn biểu diễn qua 4 số lượng tử ( cả quy mô nguyên tử Bohr và orbital ) :
Theo nguyên lý Pauli, 4 số lượng tử của từng cặp electron trong nguyên tử không được trùng nhau, giải thích cho sự phân bố của chúng trong các lớp khác nhau. Điều này cũng có nghĩa là, trên cùng một phân lớp, không có 2 electron có chiều tự quay giống nhau.
Số lượng tử chính n hình thành nên những lớp chính, trong mỗi lớp chính có n phân lớp. Các electron trên cùng một lớp thì có mức nguồn năng lượng xê dịch nhau, và trên cùng một phân lớp thì có nguồn năng lượng bằng nhau. Tổng số electron ở mỗi lớp chính phụ thuộc vào vào bộ 4 số lượng tử n, l, m và s nhưng tối đa là 2 n2 electron .Lớp electron ngoài cùng ( lớp hóa trị ) của những nguyên tố chứa những electron hóa trị, những electron này quyết định hành động những đặc thù hóa học cũng như đặc thù vật lý của chúng .
Điền electron vào những lớp[sửa|sửa mã nguồn]
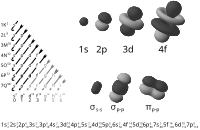 Thứ tự điền electron vào những lớp theo những mức nguồn năng lượng khác nhau
Thứ tự điền electron vào những lớp theo những mức nguồn năng lượng khác nhau
Các electron sẽ điền theo thứ tự vào các lớp có năng lượng từ thấp đến cao, bắt đầu là lớp 1s. Ngoài ra theo quy tắc Hund, các lớp electron có cùng mức năng lượng thì ban đầu được điền đơn, sao cho số electron độc thân là lớn nhất, sau đấy mới được điền đôi.
Sự điền electron vào những lớp không riêng gì phụ thuộc vào trọn vẹn vào vị trí hay khoảng cách của chúng đến hạt nhân mà còn phụ thuộc vào vào mức nguồn năng lượng của những lớp .
Ví dụ: titan có Z = 22, cấu hình theo thứ tự các lớp 1s2 2s2 2p6 3s2 3p6 3d4 4s0 nhưng do năng lượng của lớp 4s thấp hơn lớp 3d nên 4 electron còn lại sẽ điền đầy vào lớp 4s (2) trước, sau đấy mới đến lớp 3d (2), cấu hình đúng của titan là 1s2 2s2 2p6 3s2 3p6 3d2 4s2
Ngoại lệ:
- Nguyên tố lanthan, Z = 57 lớp ngoài cùng 6s2 4f1, electron tự do cuối cùng điền vào 5d trước khi vào 4f, tương tự trong nguyên tử Ac thì 6d trước 5f.
- Trong nguyên tử Cr và Cu một electron trong lớp có năng lượng thấp 4s điền vào lớp có năng lượng cao hơn 3d, chúng có cấu hình lớp ngoài cùng là 3d5 4s1 và 3d10 4s1
- Các trường hợp ngoại lệ khác Nb, Mo, Tc, Ru, Rh, Pd, Ag, Ir, Pt, Au, Gd, các actini từ Ac đến Np và Cm
18 nhóm chính (nhóm mới) trong bảng tuần hoàn được phân ra dựa theo số electron trong các lớp ngoài cùng:
- lớp s: nhóm 1 (s1) – 2 (s2)
- lớp p: nhóm 13 (p1) – 18 (p6) (Trừ He, H)
- lớp d: nhóm 3 (d1) – 12 (d10)
Số chu kỳ luân hồi bằng số lớp n, với ns là lớp ngoài cùng .
Cấu hình electron của một số nguyên tố[sửa|sửa mã nguồn]
Cấu hình electron của những nguyên tố thường được viết dưới dạng kèm theo cấu hình electron của những khí hiếm có số thứ tự nhỏ hơn đứng gần nó cộng với những lớp còn lại. Ví dụ, cấu hình electron của magiê ( Z = 12 ) : [ Ne ] 3 s2 thì được hiểu 1 s2 2 s2 2 p6 3 s2 .
| Nguyên tố | Z | Cấu hình electron |
|---|---|---|
| Heli | 2 | 1s2 |
| Neon | 10 | 1s2 2s2 2p6 |
| Argon | 18 | 1s2 2s2 2p6 3s2 3p6 |
| Krypton | 36 | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 |
| Xenon | 54 | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d105s25p6 |
| Radon | 86 | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d105s25p6 4f14 5d106s26p6 |
Z từ 1 đến 17[sửa|sửa mã nguồn]
| Nguyên tố | Z | Cấu hình electron | Cấu hình viết tắt |
|---|---|---|---|
| Hydro | 1 | 1s1 | |
| Lithi | 3 | 1s22s1 | |
| Beryli | 4 | 1s22s2 | |
| Bo | 5 | 1s2 2s2 2p1 | [He] 2s2 2p1 |
| Cacbon | 6 | 1s2 2s2 2p2 | [He] 2s2 2p2 |
| Nito | 7 | 1s2 2s2 2p3 | [He] 2s2 2p3 |
| Oxi | 8 | 1s2 2s2 2p4 | [He] 2s2 2p4 |
| fluor | 9 | 1s2 2s2 2p5 | [He] 2s2 2p5 |
| Natri | 11 | 1s2 2s2 2p6 3s1 | [Ne] 3s1 |
| Magie | 12 | 1s2 2s2 2p6 3s2 | [Ne] 3s2 |
| Nhôm | 13 | 1s2 2s2 2p6 3s2 3p1 | [Ne] 3s2 3p1 |
| Silic | 14 | 1s2 2s2 2p6 3s2 3p2 | [Ne] 3s2 3p2 |
| Phosphor | 15 | 1s2 2s2 2p6 3s2 3p3 | [Ne] 3s2 3p3 |
| Lưu huỳnh | 16 | 1s2 2s2 2p6 3s2 3p4 | [Ne] 3s2 3p4 |
| Clo | 17 | 1s2 2s2 2p6 3s2 3p5 | [Ne] 3s2 3p5 |
| Nguyên tố | Z | Cấu hình electron | Cấu hình viết tắt |
|---|---|---|---|
| Scandi | 21 | 1s2 2s2 2p6 3s2 3p6 4s2 3d1 | [Ar] 4s2 3d1 |
| Titanium | 22 | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | [Ar] 4s2 3d2 |
| Vanadi | 23 | 1s2 2s2 2p6 3s2 3p6 4s2 3d3 | [Ar] 4s2 3d3 |
| Crôm | 24 | 1s2 2s2 2p6 3s2 3p6 4s1 3d5 | [Ar] 4s1 3d5 |
| Mangan | 25 | 1s2 2s2 2p6 3s2 3p6 4s2 3d5 | [Ar] 4s2 3d5 |
| Sắt | 26 | 1s2 2s2 2p6 3s2 3p6 4s2 3d6 | [Ar] 4s2 3d6 |
| Coban | 27 | 1s2 2s2 2p6 3s2 3p6 4s2 3d7 | [Ar] 4s2 3d7 |
| Niken | 28 | 1s2 2s2 2p6 3s2 3p6 4s2 3d8 | [Ar] 4s2 3d8 |
| Đồng | 29 | 1s2 2s2 2p6 3s2 3p6 4s1 3d10 | [Ar] 4s1 3d10 |
| Kẽm | 30 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 | [Ar] 4s2 3d10 |
| Gali | 31 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p1 | [Ar] 4s2 3d10 4p1 |
Z từ 39 đến 49[sửa|sửa mã nguồn]
| Nguyên tố | Z | Cấu hình electron | Cấu hình viết tắt |
|---|---|---|---|
| Ytri | 39 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1 | [Kr] 5s2 4d1 |
| Zirconi | 40 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d2 | [Kr] 5s2 4d2 |
| Niobi | 41 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d4 | [Kr] 5s1 4d4 |
| Molybden | 42 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d5 | [Kr] 5s1 4d5 |
| Tecneti | 43 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d5 | [Kr] 5s2 4d5 |
| Rutheni | 44 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d7 | [Kr] 5s1 4d7 |
| Rhodi | 45 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d8 | [Kr] 5s1 4d8 |
| Palladi | 46 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 4d10 | [Kr] 4d10 |
| Bạc | 47 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10 | [Kr] 5s1 4d10 |
| Cadmi | 48 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 | [Kr] 5s2 4d10 |
| Indi | 49 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1 | [Kr] 4d10 5s2 5p1 |
